Quirónsalud
Blog del equipo del Dr. Meneu, Jefe de Servicio de Cirugía General y del Aparato Digestivo del CH Ruber Juan Bravo
- 20173oct
Metástasis hepáticas en cáncer de colon. Por qué el hígado primero
Dr. Juan Carlos Meneu Díaz
Introducción
El carcinoma colorrectal es el cuarto tipo más frecuente en los EEUU, por detrás del cáncer de mama, de pulmón y de próstata.
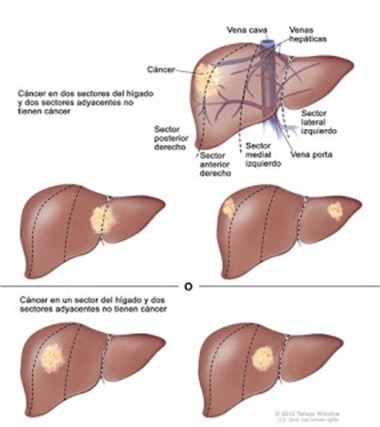
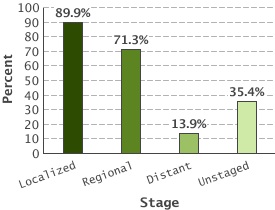
La edad media en el momento del diagnóstico es de 68 años, y la tasa de supervivencia global (incluyendo todos las etapas o estadios) es de 65% a 5 años.
En el momento de ser diagnosticados, el 39% de los pacientes presentan una fase localizada, el 36% tiene afectación regional (ganglios), y el 25% presenta metástasis en el hígado (metástasis sincrónicas), lo que representa un factor que ensombrece el pronóstico si no son tratados adecuadamente, al enfrentarnos a una enfermedad a distancia.
Tratamiento de las metástasis sincrónicas y del tumor primario.
La secuencia de tratamiento no ha sido definida claramente, y las estrategias disponibles (abordaje colorrectal inicial (ACI), abordaje colorrectal y hepático simultáneo (ACHS) ó abordaje hepático inicial (AHI), son motivo aún de controversia.
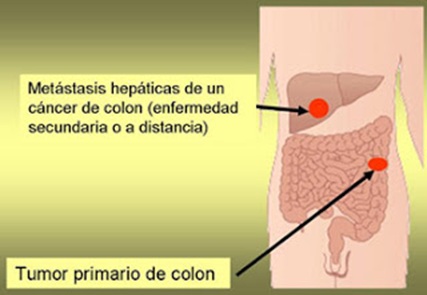
No cabe duda de que los síntomas derivados del tumor primario, en caso de existir, marcan la pauta de forma clara. Por el contrario, la mayoría de pacientes no tiene síntomas limitáneas (de colon o recto) en el momento del diagnóstico.
- Abordaje colorrectal inicial (ACI, técnica clásica).
El abordaje tradicional para este tipo de pacientes ha sido el tratamiento secuencial; primero abordar el tumor de colon y después las metástasis hepáticas. Pero este modelo presenta la desventaja del crecimiento de las metástasis que puede convertirlas en irresecables, especialmente en los pacientes que sufren complicaciones tras la cirugía colorrectal, pues así se retrasan la quimioterapia y la propia resección hepática.
- Abordaje colorrectal y hepático simultáneo (ACHS).
Por ello en la última década se ha desarrollado la resección simultánea de ambas lesiones (colon e hígado), junto con la administración de quimioterapia perioperatoria. Pero la combinación de dos cirugías de envergadura incrementa el riesgo postoperatorio.
- Abordaje hepático inicial (AHI, técnica inversa).
En el año 2006 Mentha y colaboradores propusieron el tratamiento inverso, o "abordaje hepático inical (AHI)", en el caso de metástasis hepáticas sincrónicas de carcinoma colorrectal.
Evidencia científica disponible a favor de la AHI
Disponemos de 3 estudios observacionales -nivel IV de evidencia- (1998 y 2010), publicados en la literatura científica, y una cohorte retrospectiva (nivel III de evidencia), incluyendo 121 pacientes con metástasis sincrónicas que fueron elegidas para tratamiento hepático en primer lugar (abordaje hepático inicial , AHI)
Fase de quimioterapia sistémica preoperatoria. Casi el 100% de ellos fueron tratados inicialmente con quimioterapia; el 81% de ellos presentaban un primario en el recto.
Ninguno fue intervenido de entrada del tumor de colon y sólo el 7% presentó alguna complicación relacionada con el tumor primario durante el tratamiento quimioterápico previo a la resección hepática.
Fase de cirugía en el hígado. Tras la quimioterapia sistémica de inducción el 93% de los 121 pacientes, recibió resección hepática (60% de ellas resecciones mayores, siendo el 93% de ellas R0). En relación a la cirugía hepática, la morbilidad asociada fue del 20% y la mortalidad del 1%.
Fase de cirugía en el colon o recto. A continuación se procedió a la cirugía del tumor primario de colon/recto, lo que pudo realizarse en el 74% de los pacientes, con 50% de morbilidad y 6% de mortalidad perioperatoria.
Resultados AHI. Globalmente, el 72% de los pacientes fueron sometidos a las dos fases de tratamiento. Los resultados son comparables a los obtenidos en los pacientes con metástasis hepáticas resecables, metacrónicas y una vez tratado el cáncer de colon primario. Ofrecen con una probabilidad de supervivencia a 3 años que varía entre 41%-89% y a 5 años entre 31%-89%, con riesgo de recaída de 52%.
Los resultados son similares a los obtenidos en las distintas estrategias:
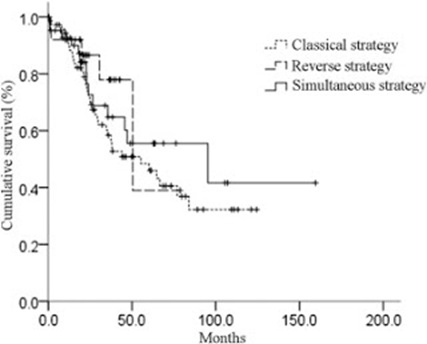
Nuestra recomendación
- El abordaje hepático inicial (AHI), debe considerarse en pacientes con carcinoma colorrectal metastásico con primario localmente avanzado, y oligosintomático o asintomático, con el objeto de tratar la enfermedad sistémica, que condiciona el pronóstico, sin dilación innecesaria.
- Este hecho es especialmente relevante en pacientes con cáncer de recto, que precisen neoadyuvancia y una intervención quirúrgica compleja, con probable confección de un estoma de protección. En estos casos, el retraso en el tratamiento sistémico, sería muy peligroso.
- 20175sep
Prevención del cáncer de colon. Pruebas de detección de carcinoma de colon. Colonoscopia virtual
Dr. Juan Carlos Meneu.
El cáncer de colon es, en nuestro país, el tumor maligno con mayor incidencia (15%) según datos de la SEOM (Sociedad Española de Oncología Médica).
En los varones, el carcinoma colorrectal (CCR) es el tercero en frecuencia, detrás del cáncer de pulmón y de próstata. En las mujeres es el segundo en frecuencia, detrás del de mama.
Según datos de la SEOM, se calcula una incidencia de 32.240 pacientes al año en España, siendo responsable de 14.700 fallecimientos y una prevalencia a cinco años de 89.705 casos.
Supervivencia en el CCR. Valor de la detección precoz
La mayoría de los casos se diagnostican entre los 65 y los 75 años, con un pico máximo a los 70 años, aunque se registran casos desde los 35-40 años. Los casos que aparecen a edades tempranas, suelen tener una predisposición genética.
En la actualidad la supervivencia relativa a 5 años en etapas localizadas es del 90,5%, mientras que en aquellos con afectación locorregional es del 71,9%, siendo del 12,5% en los que presentan metástasis a distancia.
Por tanto, el diagnóstico precoz puede tener un enorme impacto en la supervivencia de los pacientes con un CCR. La mortalidad del cáncer de colon se puede reducir mediante la detección precoz y las medidas de prevención del mismo, como es la polipectomía.

Test de sangre oculta en heces (bioquímico guaiaco-TSOH). Test inmunoquímico fecal (TIF)
Se recomienda su uso anual, en el caso de que sea el único procedimiento de cribado a realizar. Se usa en combinación con la sigmoidoscopia flexible cada 5 años, se recomienda el TSOH cada 3 años.
El TSOH no debe realizarse anualmente en combinación con la colonoscopia en los pacientes con riesgo medio de CCR. Cualquier resultado positivo, debe condicionar la realización de una colonoscopia.
La mayor desventaja de este método de cribado es que no detecta las lesiones que no sangren, que sangren poco, o de lo hagan de forma intermitente. También resulta un inconveniente, que siendo de carácter químico, el reactivo puede detectar la presencia del grupo "hemo" de carácter no humano, procedente de los alimentos ingeridos.
Para compensar estos defectos de detección, es necesario que el TSOH se realice en 3 tomas fecales sucesivas tras una estricta dieta previa.
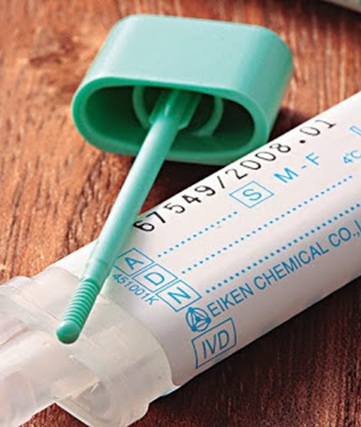
Solo deben usarse aquellos test químicos (guaiaco) con sensibilidad mayor del 70% y especificidad mayor del 90% para detectar un cáncer.
Test de detección de DNA en heces
En estudios recientes se ha demostrado que el test de detección de DNA fecal es más sensible que el TSOH o el TIF para descubrir un carcinoma colorrectal, lesiones avanzadas precancerígenas, pólipos con displasia de alto grado y pólipos serrados de > 1 cm.
Sin embargo la especificidad fue mejor con el uso de TIF y el porcentaje de pacientes excluidos por déficit de procesamiento de las muestras de DNA fue mayor que en el TIF Por este motivo, y por la falta de definición de un intervalo de realización adecuado del test, el panel de expertos del NCCN, no lo incluye en sus recomendaciones.

Colonoscopia óptica (CO)
El procedimiento de cribado más completo, al permitir la exploración de todo el colon y la resección de los pólipos en una misma sesión. Es por tanto el "gold standard" con el que se compara cualquier otro procedimiento de cribado.
Reduce la mortalidad ce cáncer de colon en más del 50%. En cada incremento de 1% en la tasa de realización de colonoscopias de cribado, se reduce el riesgo de cáncer de colon un 3%.

Se acepta que en la colonoscopia de cribado, la polipectomía debe hacerse en los pólipos de tamaño >1 cm. Por otro lado, en los pólipos diminutos (menores de 5 mm), se da la circunstancia de que resultan neoplásicos una minoría de ellos, y a su vez, <1% son avanzados histológicamente.
Por ello la Asociación Americana de Gastroenterología, ha establecido que los pólipos diminutos (< 5mm) no son causa suficiente para colonoscopia y polipectomía.
Calendario de cribado propuesto por NCCN en función de los antecedentes familiares
- Teniendo 1 Familiar de primer grado con CCR con CCR en cualquier edad: colonoscopia inicial a los 40 años (o 10 años antes de la edad de diagnóstico más precoz en la familia). Repetir la colonoscopia a intervalos de 5 años si resulta positiva en hallazgos endoscópicos
- Teniendo 1 familiar de primer grado con CCR > 60 años: colonoscopia inicial a los 50 años (o 10 años antes de la edad de diagnóstico más precoz en la familia). Repetir la colonoscopia a intervalos de 5-10 años si resulta positiva en hallazgos endoscópicos.
- Teniendo 1 familiar de segundo grado con CCR < 50 años: colonoscopia inicial a los 50 años (o 10 años antes de la edad de diagnóstico más precoz en la familia). Repetir la colonoscopia a intervalos de 5-10 años si resulta positiva en hallazgos endoscópicos.
- Teniendo 1 familiar de primer grado con adenoma avanzado (displasia de alto grado, adenoma de >1 cm, vellosos o tubulovellosos): colonoscopia inicial a los 50 años (o a la edad de diagnóstico del adenoma). Repetir la colonoscopia a intervalos de 5-10 años si resulta positiva en hallazgos endoscópicos.
Colonoscopia virtual (CV) ó colonoscopia por TAC (TAC-C)
La CV (colonoscopia virtual), tiene la ventaja de no ser invasiva y no requerir sedación, el índice de complicaciones es muy bajo y adicionalmente, puede ser más coste-eficiente que la colonoscopia óptica convencional.
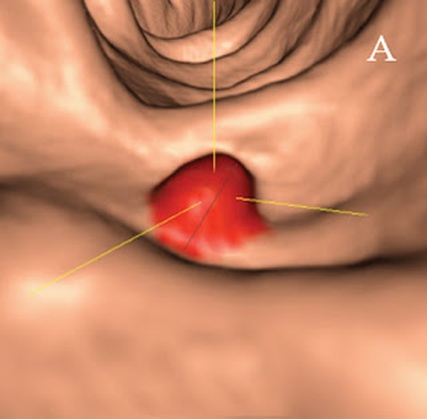
Por el contrario, cualquier hallazgo positivo en la CV, condiciona la realización de una colonoscopia óptica indefectiblemente. Y además, hasta en el 16% de los pacientes, se encuentran hallazgos patológicos extracolónicos, lo que constituye un dilema que obliga a maniobras adicionales. La sensibilidad de la CV para pólipos diminutos (< 5 mm) es 0%.
La estrategia lógica para pólipos mayores de 1 cm es la polipectomía endoscópica, la abstención en los diminutos, pero existe controversia en qué hacer con los pólipos de 6mm-9 mm.
La evidencia científica disponible demuestra que la mejor estrategia es repetir la CV cada 5 años, y referir para polipectomia endoscópica todo hallazgo de pólipos mayores de 5 mm.
- 20176jul
Patología esplénica benigna (y IV)
Dr. Fernando Trápaga Yáñez.
Traumatismos esplénicos.
El bazo es el órgano más frecuentemente lesionado en traumatismo abdominal cerrado o de la caja torácica. Su lesión exclusiva acontece apenas en el 30 % de los casos. Es por tanto habitual que se lesionen otros órganos. De más a menos frecuente estos son: caja torácica, riñón, médula espinal, hígado, pulmón, cerebro, intestino delgado, intestino grueso, páncreas, estómago.
Un tipo de traumatismo esplénico es el traumatismo quirúrgico, la lesión involuntaria del bazo en el transcurso de una gran cirugía que ocurre en un 2 % de los casos. Las cirugías más frecuentemente relacionadas con esta complicación son la gastrectomía parcial y la reparación de una hernia diafragmática.
La ruptura en dos tiempos implica la contusión esplénica con formación de un hematoma del órgano y, en un segundo tiempo, la rotura del mismo o bien espontáneamente o bien por un traumatismo banal.
La ruptura espontánea del bazo se produce por aumento de volumen del órgano que su fina cápsula no puede contener. Puede ocurrir en múltiples patologías: paludismo, mononucleosis infecciosa (causa más frecuente de muerte por virus de Epstein Barr), sarcoidosis, leucemia aguda y crónica, anemias hemolíticas, esplenomegalia congestiva, policitemia vera, candidiasis, absceso esplénico.
La tendencia quirúrgica hoy en día en relación a la ruptura del bazo es la siguiente. Bazos sanos intentar la reparación si esta es posible, sobre todo en pacientes jóvenes, y si no es posible intentar el autotransplante. En bazos enfermos proceder a la esplenectomía.
Abordaje quirúrgico del bazo.
La técnica del abordaje laparoscópico de la esplenectomía fue descrita en 1991. En ese momento las indicaciones para esplenectomía laparoscópica eran muy pocas en detrimento de las indicaciones por la vía clásica o laparotómica que eran la mayoría. En pocos años el desarrollo de las técnicas laparoscópicas ha tenido dos efectos en la cirugía del bazo. Por un lado la mayoría de las contraindicaciones absolutas de esplenectomía por vía laparoscópica han pasado a ser relativas. Y por otro lado, cuando la esplenectomía laparoscópica es posible, esta se ha ido transformando en menos invasiva si cabe (existen variantes técnicas con menos incisiones, o modalidades como la cirugía robótica que la hacen posible).
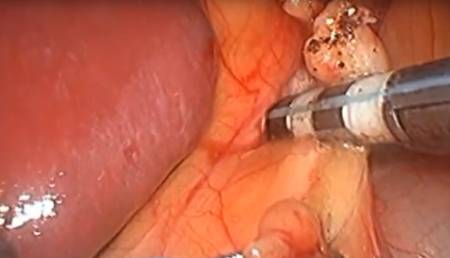
Es conveniente que la población tenga la noción de que la mayor parte de los cirujanos puede abordar un bazo por vía laparotómica, principalmente en casos de urgencia por traumatismo, pero no todos los cirujanos tienen capacidad de abordar una esplenectomía por vía laparoscópica. La cirugía del bazo es relativamente infrecuente si se compara con la cirugía de otras áreas anatómicas. Es raro encontrar cirujanos con mucha experiencia en cirugía esplénica en general, más raro aun por laparoscopia en particular. La curva de aprendizaje por laparoscopia es alta; es necesario operar muchos casos para poder tener la experiencia necesaria para ser considerado experto. Si bien es cierto que equipos con amplia experiencia en cirugía laparoscópica en otras aéreas pueden suavizar esa curva de aprendizaje. La utilización de variantes técnicas menos invasivas está reservada a los pocos cirujanos que han tenido la posibilidad de realizar muchos procedimientos por laparoscopia. Por otro lado la tasa de conversión de la vía de abordaje puede ser relativamente alta (3-8 %). Esto quiere decir que, dado que es un procedimiento difícil, es posible que un procedimiento que transcurra por vía laparoscópica termine por vía laparotómica, con buen criterio, por dificultades técnicas encontradas durante el mismo.
Actualmente las indicaciones para cirugía laparotómica son:
- Contraindicación para cirugía laparoscópica. Principalmente por causas del foro respiratorio y la imposibilidad del paciente tolerar el neumoperitoneo (la inyección de gas en la cavidad abdominal que cree una cavidad virtual que permita trabajar por laparoscopia)
- Mega bazo. Un bazo gigante, o lo suficientemente grande, no permite tener espacio suficiente para trabajar por laparoscopia.
- Trauma esplénico. Si el sangrado es lo suficientemente grande la visión por laparoscopia puede ser imposible. Recordemos que el bazo es muy vascularizado y sangra mucho.
- Por injuria o necesidad. Es decir por su lesión accidental en el transcurso de otra cirugía.
- Dentro de la técnica quirúrgica (cáncer gástrico o pancreático). Si se está operando una neoplasia con invasión del bazo se retiran los dos órganos en bloque por la misma incisión, y eso puede no ser posible por laparoscópica.
- Ptosis esplénica. La laxitud de los ligamentos que fijan el bazo a los órganos vecinos pueden condicionar una flaca exposición del órgano, dificultando o tornando peligroso realizar el procedimiento por laparoscopia.
- Bazo accesorio. La visión laparoscópica puede no detectar bazos accesorios, o aun localizados, su retirada por esta vía puede ser dificultosa.
Son contraindicaciones para el abordaje laparoscópico:
◦ Hipertensión portal.
◦ Coagulopatía.
◦ Ascitis.
El resto de indicaciones para esplenectomía, aun individualizando caso a caso, son asequibles por vía laparoscópica.
En la cirugía laparoscópica el bazo es destruido (o morcelado) dentro de una bolsa dentro de la cavidad abdominal para poder ser retirado en pequeños fragmentos. Existen situaciones, como en los tumores esplénicos, en que el bazo tiene que ser retirado íntegramente para estudio anatomopatológico. Por ello, aunque posible por vía laparoscópica, puede ser deseable la vía laparotómica. En la hidatidosis, la destrucción del bazo dentro de una bolsa puede ser arriesgada si esta se rompe, pudiendo matar al paciente por shock anafiláctico, siendo deseable retirar el órgano por una incisión lo suficientemente grande. Existen casos en los que la cirugía puede ser satisfactoria por vía laparoscópica, pero que termine por vía laparotómica, no por complicación sino por opción. La vía laparoscópica permite orientar la incisión (es lo que se denomina laparotomía dirigida).
Existen complicaciones particularmente frecuentes por vía laparoscópica. Una de ellas es la trombosis de la vena esplénica y por extensión del coágulo, la trombosis de la vena porta. Eso obliga a la profilaxis del trombo embolismo mediante la inyección subcutánea de heparinas de bajo peso molecular antes del procedimiento, y después del mismo en ocasiones por periodos relativamente prolongados. De otro modo, esta complicación ronda el 55 %.
Las complicaciones infecciosas, tanto de abscesos de la herida quirúrgica como de abscesos intra abdominales, son estadísticamente menos frecuentes por vía laparoscópica que por vía laparotómica.
Es necesario anticipar la posibilidad de hemorragia y contar con un Banco de Sangre (sangre y plaquetas) que dispense los hemo derivados en previsión antes del procedimiento. Esto es recomendable en ambas vías de abordaje.
La mortalidad de la esplenectomía electiva por vía laparoscópica es de 0.2-5 % mientras que por vía abierta es de 5-6 %.
A favor de la cirugía laparoscópica, además de lo mencionado anteriormente, hay que sumar las ventajas de esta vía de abordaje. Menor dolor postoperatorio, alta hospitalaria más precoz e incorporación más rápida a las actividades diarias. En detrimento de ella el tiempo de la realización de la cirugía es mayor y eso, juntamente con el precio del material laparoscópico puede encarecer el procedimiento si no se contabiliza el ahorro en estancia hospitalaria.
Consideraciones infecciosas post esplenectomía.
Los pacientes esplenectomizados son más sensibles a ciertas infecciones y es necesario proceder a vacunarlos.
- Bacterias encapsuladas: streptococcus pneumoniae (50 %). Se caracteriza por neumonía en adultos y meningitis en niños.
Vacuna anti neumocócica polisacarídica.
– 1 dosis inicial. 2 semanas antes de un procedimiento electivo o inmediatamente antes de un procedimiento urgente.
– Repetir cada 3-5 años.
- Haemophilus influenzae (20-30 %). Se ha descrito la sepsis letal por gripe en niños en un 2-7 % de los casos.
Vacuna antigripal anual.
- Neisseria meningitidis.
Vacuna tetravalente ACYW 135 o bivalente A+C
Vacuna anti meningocócica C conjugada
- 20177jun
Patología esplénica benigna (III)
Dr. Fernando Trápaga Yáñez.
Trastornos hematológicos.
Existen trastornos de los eritrocitos que hacen que sean destruidos en el bazo provocando anemia. Algunos de ellos pueden ser tratados mediante esplenectomía.
Intracelulares:
◦ Defectos de membrana.
◦ Defectos enzimáticos.
◦ Hemoglobinopatías.
Extracelulares:
◦ Anemia hemolítica inmune.
◦ Púrpura trombocitopénica idiopática.
◦ Púrpura trombocitopénica trombótica.
Los defectos de membrana son la esferocitosis, la eliptocitosis y la estomatocitosis. Todos ellos son congénitos. La esferocitosis es la anemia hemolítica familiar más frecuente. Cursa con anemia, ictericia y esplenomegalia. Generalmente es poco sintomática pero puede manifestarse en forma de crisis (dolor abdominal, fiebre, vómitos y taquicardia) exacerbadas por infección (viral), stress, fatiga o hipotermia. Existe colelitiasis en un 60 %. Y úlceras crónicas de los miembros inferiores en casos raros.
El tratamiento de la esferocitosis es la esplenectomía. Hay que buscar bazos accesorios y retirarlos cuando existen. Tras la esplenectomía el defecto de membrana persiste, a pesar de lo cual, las úlceras de los miembros inferiores se curan. La eliptocitosis y la estomatocitosis responden peor a la esplenectomía.
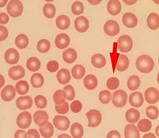
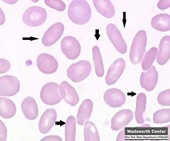
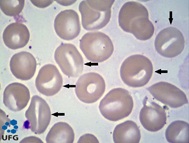
Los defectos enzimáticos son dos. Tipo I o déficit de Glucosa 6 fosfato desidrogenasa (G6PD) y tipo II o déficit de Piruvatoquinasa. Ambos son clínicamente indistinguibles. La clínica es variable. La mayor parte son niños asintomáticos pero puede ser desencadenado por infecciones, fármacos y habas (fabismo). Cursa con anemia, ictericia neonatal (retraso mental y muerte), esplenomegalia (más frecuente en tipo II). La colelitiasis es frecuente. Los casos graves causan insuficiencia renal y muerte.
El tratamiento pasa por evitar las substancias desencadenantes de las crisis. La esplenectomía se ofrece en casos con el tipo II que son sintomáticos. Este tipo de intervención ha de ser muy bien ponderado en primer lugar porque las infecciones en niños sin bazo son más frecuentes y graves, y en segundo lugar por una iatrogenia que se puede producir; la trombocitosis secundaria a la esplenectomía puede causar trombosis de la vena porta o de la vena cava
La talasemia o anemia mediterránea o de Cooley es un tipo de hemoglobinopatía. Hay varios tipos (alfa, beta y gamma). En ella hay agregados de hemoglobina alterada (cuerpos de Heinz) que provocan su interceptación y destrucción en el bazo.
La clínica es variable. Suelen ser niños con síntomas variables que van desde el estado asintomático hasta anemia, ictericia y esplenomegalia, colelitiasis, ulceras cutáneas y micro infartos esplénicos.
El tratamiento pasa por terapia transfusional hasta esplenectomía en los casos más graves.

Otra hemoglobinopatía frecuente es la drepanocitosis o anemia de células falciformes. El rasgo falciforme afecta al 9 % de la raza negra aunque sólo causa anemia en 0,3-1,3 % de los casos. Se considera protector contra la malaria.
En hipoxemia (falta de oxígeno en la sangre), el eritrocito se deforma. La sangre se torna más espesa, obstruyendo los capilares y agravando la hipoxemia. Se producen micro infartos: dolor óseo, priapismo (erección dolorosa), daño neurológico, úlceras de pierna. Inicialmente hay esplenomegalia, por último hay fibrosis (auto esplenectomía por los infartos) o bien abscesos esplénicos: dolor, fiebre y esplenomegalia.
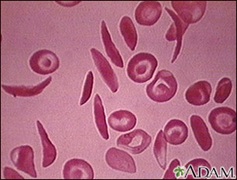
Entre los defectos extracelulares están la anemia hemolítica inmune, la púrpura trombocitopénica idiopática, el síndrome de Evans (la suma de los dos anteriores), y la púrpura trombocitopénica trombótica. Todos ellas son enfermedades autoinmunes donde anticuerpos circulantes se fijan o a los eritrocitos o al endotelio vascular provocando la destrucción de las células sanguíneas.
La anemia hemolítica inmune (AHAI) es el doble de frecuente en mujeres que en hombres. Ocurre a los 50 años y la clínica puede ser insidiosa o fulminante. Se caracteriza por anemia, ictericia, esplenomegalia (25 %) e insuficiencia renal por filtración renal de hemoglobina en exceso. El diagnóstico se basa en la detección laboratorial de los anticuerpos (test de Coombs). Hay tres tipos: anticuerpos fríos, anticuerpos calientes (70 %), e inducida por fármacos. El tratamiento es inicialmente médico (corticoides). La esplenectomía está indicada cuando falla el tratamiento médico, cuando las dosis de corticoides son inaceptablemente altas, cuando existen efectos secundarios del tratamiento médico y cuando existe contraindicación del uso de corticoides. La esplenectomía se debe ofrecer a los pacientes con la variedad de anticuerpos calientes que tengan una relación del secuestro espleno-hepático de eritrocitos marcados con Cr51 de 2:1 o 3:1.
La púrpura trombocitopénica idiopática (PTI) o inmune es la Indicación hematológica más frecuente de esplenectomía. Es una enfermedad que afecta tres veces más a las mujeres. El bazo produce anticuerpos IgG anti-plaquetas y fagocita plaquetas. La clínica se manifiesta por pequeñas hemorragias cutáneas (petequias) y equimosis (hematomas). Existen hemorragias gastrointestinales (gingival, de úlcera péptica, hemorroidal, etc.), urológicas (hematuria), ginecológicas (cíclicas al principio del ciclo) e incluso neurológicas. Como trastorno autoinmune que es se asocia al lupus eritematoso sistémico. Los pacientes con SIDA tienen mayor incidencia de esta enfermedad. En la PTI las plaquetas son <50.000/mm³, el tiempo de sangría es alto y las pruebas de coagulación son normales.
Tratamiento.
◦ Niños (lo más común,
◦ Adultos (insidioso, >6 meses). Apenas 15 % mejora con tratamiento médico por tanto se recurre a la esplenectomía en el 75-80 % de los casos.
La púrpura trombocitopénica trombótica (PTT) es una enfermedad autoinmune de arteriolas y capilares. Se caracteriza por inicio rápido y fulminante. Sus manifestaciones son fiebre, púrpura, anemia hemolítica, alteraciones neurológicas y nefropatía. Existe esplenomegalia en un 20 %. 5 % ocurre en el embarazo. El tratamiento inicial es médico. En casos más graves se tiene que recurrir a plasmaféresis y esplenectomía.
Patología esplénica benigna - trastornos hematológicos - esferocitosis - eliptocitosis y estomatocitosis - talasemia o anemia mediterránea o de Cooley - drepanocitosis o anemia de células falciformes - anemia hemolítica inmune - púrpura trombocitopénica idiopática - síndrome de Evans y púrpura trombocitopénica trombótica - Dr. Fernando Trápaga Yáñez - Dr. Juan Carlos Meneu - complejo hospitalario Ruber Juan Bravo0 comentarios - 201711may
Patología esplénica benigna (II)
Dr. Fernando Trápaga Yáñez
Quistes esplénicos.
Los quistes parasitarios representan 2/3 de todos los quistes del bazo mientras que el tercio restante son no parasitarios.
Aunque existen cuatro especies de parásitos capaces de hacer enfermar a los humanos, en la Península Ibérica los quistes parasitarios son causados por el microorganismo echinococcus granulosus y son comúnmente conocidos como quistes hidatídicos. La hidatidosis afecta principalmente al hígado (65 %) y al pulmón (25 %). El 10 % restante afecta a otros órganos (corazón, cerebro, huesos y también el bazo). Varios órganos se pueden ver afectados.
El parásito vive en el intestino delgado de perros, lobos y zorros. El animal desprende los huevos del parásito por las heces que contaminan los campos donde pasta ganado de cierto porte, principalmente ovino. No ha de extrañar que en un país donde la trashumancia fue tan importante la hidatidosis haya sido en el pasado una enfermedad frecuente. Las ovejas pastan hierba contaminada y desarrollan la enfermedad. El ser humano perpetúa el ciclo al alimentar a los canes con las vísceras de las ovejas enfermas y se infecta secundariamente por el contacto con el pelaje del perro contaminado por los huevos del parásito.
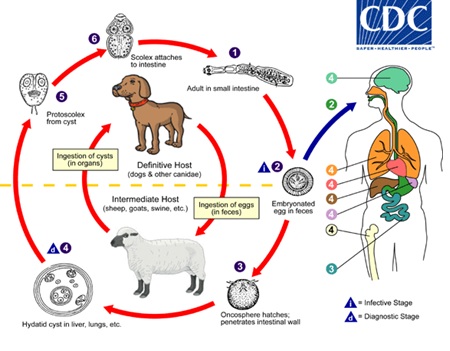
En los países del norte de Europa, Estados Unidos, Rusia, China y Japón, el parásito causante es el echinococcus multilocularis. El parásito vive en el intestino de zorros, coyotes, perros y gatos que se alimentan de roedores enfermos de hidatidosis. El ser humano se contagia secundariamente así como el ganado porcino y equino. Esta variante de hidatidosis afecta principalmente al hígado.
En América del Sur hay dos especies de echinococcus, vogeli y oligarthrus capaces de causar hidatidosis en humanos. Si bien están más restringidos a zonas tropicales, los fenómenos migratorios pueden motivar que aparezcan casos aislados en España.
El diagnóstico en el pasado se basaba en la prueba cutánea de Casoni. Se esterilizaba el contenido líquido de un quiste y se inyectaba subcutáneamente provocando una reacción alérgica en la piel. Representa la memoria inmunológica del individuo hacia el parásito, pero no discrimina la actividad de la enfermedad. Es decir, no especifica si la infección es actual o remota y si es activa o si el paciente ya se curó.
Actualmente el diagnóstico se basa en estudios serológicos (Ig E) y en estudios de imagen (principalmente ecografía y TAC)
El tratamiento médico de la enfermedad (mebendazol, albendazol, flubendazol) tiene una baja eficacia, se administra durante tiempo prolongado y no está exento de efectos secundarios. Cuando la afectación es exclusiva del bazo, lo que es raro, el tratamiento de elección es la esplenectomía que se puede complementar con medicación para intentar evitar las recidivas.
La ruptura de los quistes durante la cirugía y el derrame del contenido de los mismos (rico en parásitos) en el peritoneo puede producir un shock anafiláctico de consecuencias mortales sin tratamiento. Existe la posibilidad de esterilizar los quistes mediante la inyección de cloruro de sodio al 3%, antes de su manipulación quirúrgica.
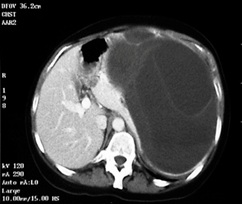
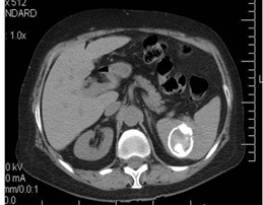
En estas dos imágenes observamos un quiste hidatídico gigante activo y un quiste hidatídico calcificado e inactivo.
Los quistes no parasitarios pueden ser:
◦ Seudoquistes 70-80%.
◦ Quistes congénitos simples.
◦ Quistes epidermoides.
Los seudoquistes se llaman así por no tener una cápsula epitelial. Son adquiridos y se producen como consecuencia de un traumatismo que provoca un hematoma, una colección de sangre dentro del bazo. La resolución del hematoma causa el seudoquiste. Son generalmente asintomáticos, y cuando alcanzan gran tamaño dan síntomas por compresión de órganos vecinos. El 25% de los casos se complican con ruptura, infección o hemorragia significativa.
El tratamiento puede ser expectante en casos de seudoquistes pequeños o no complicados. En caso contrario el tratamiento es quirúrgico. Las opciones quirúrgicas van desde destechamiento del quiste y drenaje, hasta esplenectomía (parcial o total).
Los quistes simples y los quistes epidermoides son mucho más raros, existen pocos casos descritos en la literatura. Ambos son congénitos y se caracterizan por tener un revestimiento epitelial. En el caso de los quistes epidermoides, además, contienen estructuras propias de la piel. Sus complicaciones son las mismas que las de los seudoquistes, a las que hay que sumar el potencial de malignización (raro) de ese epitelio. Es difícil diferenciar un quiste de un seudoquiste. El diagnóstico diferencial solo lo puede hacer la biopsia. Por tanto, si no se decide una actitud expectante, el tratamiento correcto sería la esplenectomía (parcial o total).
Aneurisma de la arteria esplénica
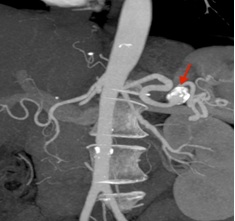 Se trata de una enfermedad poco frecuente que afecta al 0,02-0,16 % de la población. A pesar de ser raro, representa la localización más frecuente de aneurisma abdominal si excluimos los aneurismas de aorta.
Se trata de una enfermedad poco frecuente que afecta al 0,02-0,16 % de la población. A pesar de ser raro, representa la localización más frecuente de aneurisma abdominal si excluimos los aneurismas de aorta.Ocurre generalmente en mujeres en su 6ª década de vida que han tenido de 4 a 5 embarazos de media. Puede ser único o múltiple. Suelen tener unos 3 cm de diámetro de media aunque
Son asintomáticos en el 80 % de los casos. Suele haber calcificación de la pared del aneurisma y asociación con arterioesclerosis. Cuando dan síntomas, el más frecuente es el dolor abdominal. El riesgo de rotura es raro; rompe uno de cada más de treinta. Un 12 % de los que rompen tienen un sangrado limitado o contenido antes de romper definitivamente, el resto lo harán directamente de forma masiva o al peritoneo (lo más común) o al tubo digestivo (estómago, colon o intestino delgado) en forma de fistulización y hemorragia digestiva. Un caso particular es la rotura en mujeres embarazadas (lo que ocurre en el tercer trimestre en el 70% de los casos) porque tiene una mortalidad del 70 % para la madre y del 95 % para el feto.
El diagnóstico se hace frecuentemente por TAC y arteriografía.
El tratamiento es quirúrgico en los siguientes casos:
- Mayores de 2 cm.
- Sintomáticos.
- Antes del embarazo, o antes del tercer trimestre del embarazo.
Las opciones quirúrgicas son la resección del aneurisma (el bazo sobrevive a la sección de la arteria esplénica, 80 % de su aporte, si se respetan los vasos gástricos cortos, 20 % de su aporte) si el aneurisma es único y proximal a la aorta, o la esplenectomía si los aneurismas son múltiples o único en el hilio esplénico.
Bienvenido al blog del Servicio de Cirugía General y del Aparato Digestivo del Complejo Hospitalario Ruber Juan Bravo. Este espacio está creado para aconsejar e informar sobre las enfermedades del aparato digestivo, de la cirugía general, de la cirugía laparoscópica, de la cirugía robótica, de la cirugía de la carcinomatosis, de la cirugia endocrina, de la cirugía metabólica y de la obesidad, de la cirugía de colon y de recto y de la proctología, ademas de la cirugía oncológica, entre otros aspectos. El cáncer del aparato digestivo es una de las principales causa de muerte en todo el mundo. Estamos abiertos a responder a cualquier duda o cuestión. Será un placer intentar resolverla.
 2.024
2.024
 2.023
2.023
 2.022
2.022
 2.021
2.021
 2.020
2.020
 2.019
2.019
 2.018
2.018
 2.017
2.017
 2.016
2.016
La finalidad de este blog es proporcionar información de salud que, en ningún caso sustituye la consulta con su médico. Este blog está sujeto a moderación, de manera que se excluyen de él los comentarios ofensivos, publicitarios, o que no se consideren oportunos en relación con el tema que trata cada uno de los artículos.
Quirónsalud no se hace responsable de los contenidos, opiniones e imágenes que aparezcan en los "blogs". En cualquier caso, si Quirónsalud es informado de que existe cualquier contenido inapropiado o ilícito, procederá a su eliminación de forma inmediata.
Los textos, artículos y contenidos de este BLOG están sujetos y protegidos por derechos de propiedad intelectual e industrial, disponiendo Quirónsalud de los permisos necesarios para la utilización de las imágenes, fotografías, textos, diseños, animaciones y demás contenido o elementos del blog. El acceso y utilización de este Blog no confiere al Visitante ningún tipo de licencia o derecho de uso o explotación alguno, por lo que el uso, reproducción, distribución, comunicación pública, transformación o cualquier otra actividad similar o análoga, queda totalmente prohibida salvo que medie expresa autorización por escrito de Quirónsalud.
Quirónsalud se reserva la facultad de retirar o suspender temporal o definitivamente, en cualquier momento y sin necesidad de aviso previo, el acceso al Blog y/o a los contenidos del mismo a aquellos Visitantes, internautas o usuarios de internet que incumplan lo establecido en el presente Aviso, todo ello sin perjuicio del ejercicio de las acciones contra los mismos que procedan conforme a la Ley y al Derecho.